Đại diện Cục Quản lý dược trả lời hội đồng xét xử, đã cấp phép “đúng quy trình”.
Chiều 24/10, sau 4 ngày xét xử, phiên phúc thẩm vụ án Nguyễn Minh Hùng, Võ Mạnh Cường và đồng phạm buôn lậu thuốc chữa bệnh và làm giả con dấu, tài liệu của cơ quan, tổ chức xảy ra tại Công ty CP VN Pharma (Q.10, TP.HCM) đã tạm khép lại với phần nghị án dài ngày, do tính chất phức tạp và quy mô của vụ án. Dự kiến, Hội đồng xét xử (HĐXX) TAND Cấp cao tại TP.HCM sẽ tuyên án vào ngày 30/10 tới.
Đề nghị hủy án, khởi tố hành vi buôn bán thuốc giả
Bảo vệ quan điểm của quyết định kháng nghị số 20/QĐ-VC3-V1 do Viện trưởng Viện kiểm sát (VKS) nhân dân Cấp cao tại TP.HCM ký ban hành, đại diện VKS cho rằng, bản án sơ thẩm đã tuyên xử các bị cáo về tội buôn lậu và làm giả con dấu, tài liệu của cơ quan, tổ chức là chưa đầy đủ, chưa toàn diện và chưa phản ánh đúng bản chất vụ án, có dấu hiệu bỏ lọt hành vi phạm tội và người phạm tội.
 |
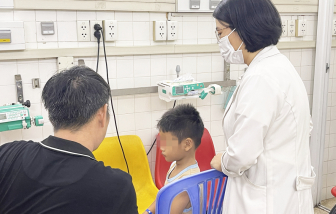
| Đại diện Bộ Y tế tại toà ngày 24/10 - Ảnh: Quốc Ngọc |
Kháng nghị đặt vấn đề trách nhiệm các cá nhân của Cục Quản lý dược (CQLD) có liên quan trong việc thẩm định hồ sơ và cấp phép nhập khâu lô thuốc H-Capita. Theo đó khẳng định, cấp sơ thẩm chưa làm rõ trách nhiệm quá trình cấp phép nhập khẩu lô thuốc H-Capita và 3 lô thuốc khác đã nhập vào Việt Nam của cục.
Bên cạnh lô thuốc H-Capita được sản xuất bởi Công ty “ma” Helix Pharmaceuticals Inc (Canada), đại diện VKS phát biểu bổ sung kháng nghị cho rằng, đơn đặt hàng có mã số, mã vạch khác nhau, giấy phép hoạt động của Công ty Austin Hồng Kông (đơn vị cung cấp) hết hạn, có đến 3/10 chuyên gia tham gia tổ giám định lô thuốc H-Capita không ký tên vào biên bản, lượng tạp chất của thuốc là 0,17%... nhưng CQLD vẫn ký giấy phép nhập khẩu cho VN Pharma là vi phạm nghiệm trọng. Đề nghị cần phải điều tra làm rõ các vi phạm này.
Theo đại diện VKS, qua phần xét hỏi tại tòa, càng chứng minh kháng nghị của VKS hoàn toàn có cơ sở và đề nghị HĐXX chấp nhận toàn bộ kháng nghị, hủy án sơ thẩm, trả hồ sơ điều tra lại vụ án.
Ngoài ra, theo VKS, thuốc kém chất lượng được quy định là thuốc không đạt tiêu chuẩn chất lượng đã đăng ký với cơ quan có thẩm quyền. Thuốc giả là sản phẩm được sản xuất dưới dạng thuốc với ý đồ lừa đảo, thuộc một trong những trường hợp không có dược chất, có dược chất nhưng không có hàm lượng đã đăng ký, có dược chất khác với dược chất ghi trên nhãn…
Thế nhưng, kết luận giám định của Bộ Y tế lại có nhiều mâu thuẫn, không phù hợp với quy định pháp luật và thực tế khách quan của vụ án. Cụ thể, kết luận giám định cho rằng, lô thuốc H-Capita chứa 97,5% hoạt chất Capecitabine không rõ nguồn gốc, kém chất lượng, không được sử dụng làm thuốc chữa bệnh cho người.
Trong khi các bị cáo nhập về với mục đích chữa bệnh ung thư cho người. Và cũng chính kết luận lại cho rằng, đây là thuốc kém chất lượng mà không kết luận là thuốc giả, theo VKS là quá mâu thuẫn.
 |
| Ảnh: Minh Thanh. |
Qua phân tích, đại diện VKS cho rằng, hành vi của các bị cáo có dấu hiệu phạm tội sản xuất, buôn bán hàng giả là thuốc chữa bệnh, đề nghị cần khởi tố điều tra làm rõ.
Chỉ căn cứ vào tài liệu doanh nghiệp cung cấp để cấp phép (?)
Liên quan trực tiếp tới vụ án, tại phiên tòa ngày 24/10, nhiều lần tên của Thứ trưởng Bộ Y tế kiêm Cục trưởng CQLD Trương Quốc Cường được HĐXX xướng lên, nhưng ông này vẫn không có mặt với lý do “không nhận được thư mời của tòa”.
Trả lời các câu hỏi của chủ tọa về quy trình cấp phép cho VN Pharma nhập thuốc H-Capita cũng như chứng cứ mới về việc cấp phép cho Công ty “ma” Helix Pharmaceuticals Inc (Canada) hoạt động tại Việt Nam, đại diện CQLD đều khẳng định đã làm “đúng quy trình”.
Theo hồ sơ chúng tôi có được, giấy phép hoạt động số 28/GP-2014/2 của doanh nghiệp nước ngoài về thuốc và nguyên liệu làm thuốc tại Việt Nam do chính ông Trương Quốc Cường ký tên cấp cho Công ty Helix Pharmaceuticals Inc (Canada) ngày 18/6/2014, có hiệu lực đến ngày 18/6/2019.
Tuy nhiên, kết luận điều tra và cáo trạng lại thể hiện, Bộ Công thương xác định mã số, mã vạch in trên vỏ hộp thuốc H-Capita không được đăng ký bởi quốc gia nào. Kết quả giám định giấy chứng nhận bán hàng tự do (FSC) tại Canada của thuốc H-Capita và giấy chứng nhận thực thành tốt sản xuất thuốc (GMP) do Bộ Y tế Canada cấp cho Công ty Helix Pharmaceuticals Inc là giấy giả.
Ngày 30/9/2014, Bộ Ngoại giao có Công văn số 1958/BNG-CM-m gửi Cục An ninh chính trị nội bộ (Bộ Công an) trả lời kết quả xác minh địa chỉ 392 Wilson Ave, Toronto, Ontario, Canada không hề có công ty nào tên là Helix Pharmaceuticals Inc, cũng như không có số, ngày đăng ký kinh doanh như giấy tờ đã nộp cho CQLD.
 |
| Ảnh: Hiếu Nguyễn. |
Ấy thế mà, theo tìm hiểu của chúng tôi, để được cấp giấy phép hoạt động số 28/GP-2014/2 nêu trên, doanh nghiệp phải trải qua quy trình “chặt chẽ” của Bộ Y tế. Đầu tiên, doanh nghiệp gửi hồ sơ đăng ký về CQLD với phí thẩm định 15 triệu đồng/lần. Cục tiếp nhận, thẩm định hồ sơ và trình hội đồng xét duyệt. Sau đó, có quyết định cấp phép hoặc chưa cấp và trả kết quả cho doanh nghiệp.
Hồ sơ phải hội đủ: đơn đăng ký doanh nghiệp nước ngoài hoạt động về thuốc tại Việt Nam, hồ sơ tóm tắt hoạt động của doanh nghiệp (theo mẫu của Thông tư 47/2011/TT-BYT), các tài liệu chứng minh việc thành lập doanh nghiệp tại nước sở tại (trong đó có chức năng sản xuất và/hoặc buôn bán thuốc.
Đối với doanh nghiệp là nhà sản xuất, phải có GMP hoặc chứng nhận sản phẩm dược (CPP) theo hệ thống chứng nhận của Tổ chức Y tế thế giới (WHO). Nếu là doanh nghiệp phân phối thì phải là doanh nghiệp được phép buôn bán, xuất nhập khẩu, bảo quản thuốc do cơ quan quản lý có thẩm quyền của nước sở tại cấp. Cuối cùng là văn bản xác nhận của cơ quan thuế (nơi doanh nghiệp đăng ký hoạt động).
Lạ thay, với hàng loạt thủ tục “kín kẽ” như trên, không hiểu tại sao CQLD lại có thể cấp phép cho một công ty “ma” hoạt động. Nghiêm trọng hơn, đại diện của CQLD - cơ quan được giao trọng trách quản lý nhà nước đối với việc cấp phép này - lại có thể khẳng định trước tòa, rằng họ đã không xác minh tính hợp pháp của hồ sơ. Họ chỉ căn cứ vào các tài liệu do doanh nghiệp cung cấp, để cấp phép (?).
Như chúng tôi đã đưa tin, luật sư của các bị cáo lập luận, hồ sơ xin cấp giấy phép này đã được Bộ Y tế chấp thuận và đồng ý cấp cho phép hoạt động tại Việt Nam, cho thấy bộ đã thừa nhận sự tồn tại trên thực tế của… công ty “ma”. Xem ra, mức độ của sai phạm giữa các bị cáo và các cá nhân ở CQLD liên quan, là ngang nhau? Thế nhưng, hiện mới chỉ có một phía đứng trước vành móng ngựa, vì sao?
Quốc Ngọc